Povijesna literatura opisuje toksične učinke gljiva još iz antičkog doba. U sedmom i osmom stoljeću prije Krista, održao se Robigalia festival posvećen bogu Robigusu, bogu koji štiti usjeve i stabla tijekom proljeća kada se očekuje da će usjevi biti napadnuti „hrđom“ i plijesnima. I u Starom zavjetu (Levitski zakonik 14:37-45) opisana je prisutnost zelene ili crvene plijesni na zidovima kuća. Prva dokumentirana mikotoksikoza pojavljuje se u Srednjem vijeku tijekom epidemije sa simptomima halucinacije, delirija, konvulzija i gangrene znane kao Vatra Svetog Antuna. Do 1850. god. bolest je prozvana ergotizam, uzrokovana je gljivom raževa glavnica – Claviceps purpurea var. Purpurea. Godine 1948. Freeman je izolirao prvi trihotecen mikotoksin iz plijesni Trichothecium roseum. Trihotecen mikotoksin, T-2 toksin, bio je sumnjiva etiološka tvar za brojna otrovanja hranom izazivajući leukopeniju u Rusiji tijekom zadnjih godina Drugoga svjetskog rata. Interes za mikotoksikozama raste nakon izolacije mikotoksina aflatoksina iz plijesni Aspergillus flavus u ugandanskom kikirikiju u kasnim 1950-ima. Konzumacija takvog kontaminiranog kikirikija na farmama izazvala je ugibanje stotina tisuća purica i pataka u ranim 1960-tim. Sljedeći otkriveni mikotoksin je aflatoksin B1 za kojega se pretpostavilo da je prirodni karcinogen. Svjetska zdravstvena organizacija navela je još tri klase mikotoksina (okratoksin, zearalenon, trihotrihoteceni) kao potencijalno štetne tvari za zdravlje ljudi i životinja. Godine 1965. izoliran je okratoksin A iz plijesni Aspergillus alutaceus. Tijekom nekoliko zadnjih desetljeća zabilježene su mikotoksikoze uključujući hepatitis uzrokovan konzumacijom kukuruza s aflatoksinom u Keniji i Indiji, gastroenteritis uzrokovan konzumacijom prosa kontaminiranog raževom glavnicom u Indiji i diareja povezana s konzumacijom sirka i kukuruza kontaminiranim fumonizinom B1.
Mikotoksini (gr. mykes – gljiva, toxicon – otrov), kao česti onečišćivači hrane, uz brojne značajne štete u gospodarstvu, uzročnici su različitih bolesti, najčešće putem hrane, rjeđe respiratornim putem. Bolesti koje prouzročuju su mikotoksikoze. Predstavljaju veliki problem za ljude i životinje u brojnim zemljama te, ovisno o načinu unosa u organizam, mogu biti primarne i sekundarne. Mikotoksini su kemijski spojevi različite strukture, različitog biološkog učinka, u pravilu bez boje i okusa. Posjeduju visoku akutnu toksičnost, često povezanu uz maligne bolesti (karcinogenost, mutagenost, imunotoksičnost, hepatotoksičnost, nefrotoksičnost, fenotoksičnost, dermatotoksičnost, hematotoksičnost, teratogenost). Velika je zabrinutost prisutna zbog karcinogenosti i kronične izloženosti i ljudi i životinja većini mikotoksina. Prema djelovanju na organizam i bolestima koje izazivaju, razlikuju se:
a) Nefrotoksini (okratoksini, citrinin i dr.)
b) Neurotoksini (patulin, fumonizini i dr.)
c) Hepatotoksini (aflatoksini, sterigmatocistin, grizeofulvin i dr.)
d) Estrogeni (zearalenon)
e) Citotoksini (trihoteceni)
f) Imunosupresori (okratoksini, trihoteceni, gliotoksin)
g) Respiratorni (fumonizini, trihoteceni, stahibotritoksin)
h) Fotosenzibilizirajući (sporidezmini)
i) Skupina povezana uz odbijanje hrane (deoksinivalenol, diacetoksiscirpenol)
Mikotoksini su stabilni i u pravilu otporni na povećanu temperaturu. Njihova biosinteza ovisi o vrsti toksikotvorne plijesni, o klimatskim i okolišnim uvjetima, fizikalno – kemijskim čimbenicima (temperaturi: -5 do 60°C, sadržaju vode u namirnici: 13% i više, pH vrijednosti: 3 – 9 te koncentraciji plinova u atmosferi i sastavu namirnice).
Od dvjestotinjak do sada poznatih mikotoksina, najznačajniji po svome toksičnom i karcinogenom učinku jesu: aflatoksini (AFB1, AFM1), okratoksini (OTA), zearalenon (ZEA, F-2), fumonizini (FB1, FB2), trihoteceni (T-2 toksin), patulin (PAT). Poznato je da dvadesetak različitih patogenih plijesni ima sposobnost proizvodnje dvaju ili više različitih mikotoksina. Do nastanka mikotoksikoze dolazi izravnim ili neizravnim stalnim unosom mikotoksina u manjim koncentracijama putem mikotoksinom onečišćene hrane. Sumnja na mikotoksikoze u ljudi je prisutna, ukoliko se neka od bolesti izazvana mikotoksinima pojavljuje u većem broju ljudi.
Otrovanja mikotoksinima, ovisno o izloženosti hrani onečišćenoj mikotoksikotvornim plijesnima, mogu biti akutna, kao posljedica jednokratnog uzimanja namirnica s visokom do umjerenom koncentracijom mikotoksina i/ili kronična, nastala konzumiranjem namirnica s umjerenim do malim koncentracijama mikotoksina tijekom dužega vremenskog razdoblja (s mogućim letalnim završetkom).
Pojavljuju se u zemljama lošega socijalno – ekonomskog stanja i lošega poljoprivredno – veterinarskoga standarda, posebice kod uzgoja, transporta i uskladištenja hrane biljnoga i animalnoga podrijetla. Također, onečišćenje zraka aflatoksinom u industrijskim prostorima za proizvodnju hrane u nekim zemljama Europe u više slučajeva bilo je povezivano s malignim bolestima dišnih putova.
Simptomi mikotoksikoza ovise o brojnim čimbenicima: starosnoj dobi i spolu, vrsti i koncentraciji mikotoksina, vremenu izloženosti, farmakodinamičkim osobinama (distribuciji u tkivu, odnosno organu, njegovome metabolizmu, poluvremenu raspada te učinkovitosti organizma u pogledu njihovog uklanjanja). Njihove karakteristike jesu: bolest nije prenosiva; povezana je uz određenu vrstu hrane ili uz promjenu prehrane; liječenje lijekovima i antibioticima je bez rezultata; iako su neki simptomi slični avitaminozi, liječenje vitaminima nije učinkovito; bolesti su sezonske prirode (zbog klimatskih uvjeta koji utječu na rast i razmnožavanje plijesni).
U cilju sprečavanja moguće kontaminacije hrane toksikotvornim plijesnima i mikotoksinima, potrebno je poznavati preventivne mjere za sprečavanje kontaminacije; fizikalne, kemijske i biološke preventivne mjere, mjere uzgoja, žetve i pohrane krme i žitarica te mjere u proizvodnom procesu, transportu i pri uskaldištenju.
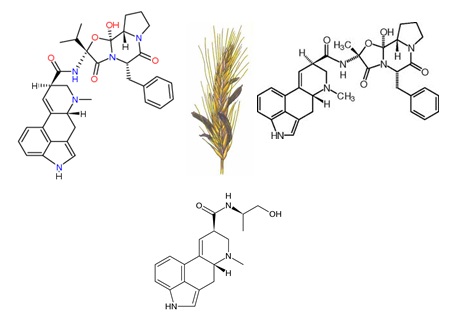
Termin ergotoksini odnosi se i na produkte sklerocija plijesni Claviceps purpurea i na ergolinske alkaloide unutar sklerocija (sklerocij je tvrda micelarna nakupina, građena od pseudoparenhima i omotana čvrstom sklerotiziranom korom). Služi gljivi za preživljavanje nepovoljnih uvjeta u prirodi (karakteristično za rod Sclerotinia). Nađeni su sklerociji bez alkaloida ili u tragovima, kao i sklerociji s vrlo velikim sadržajem alkaloida (oko 1,5%). Iz raževe glavnice izolirano je više od 30 alkaloida. Svi prirodni ergolinski alkaloidi (ergolini) amidni su derivati tetracikličkog spoja 6 – metil-ergolina koji u svojoj strukturi ima lizerginsku kiselinu. Alkaloidi su svrstani u dvije velike skupine: 1. alkaloidi lizerginske kisline i 2. klavinski alkaloidi. Prvoj skupini pripadaju ergolinski alkaloidi u Claviceps purpurei (primarno derivati lizerginske i izolizerginske kiseline), a drugoj skupini ergolinski alkaloidi iz Claviceps fusiformis (primarno derivati dimetilergolina, klavini.
Posebnu skupinu ergotoksina izoliranih u malim količinama iz raževe glavnice čini skupina 12 klavinskih alkaloida (klavina). Sklerocij ražene glavnice sadrži i druge tvari koje utječu na kroničnu toksičnost raževe glavnice.
Spore gljiva nošene vjetrom dolaze do plodnica mlade raži gdje hifama ulaze duboko u tkivo i tvore ljubičasto-crne ili ljubičasto-crvene sklerocije. Sklerociji se formiraju na mjestu cvata te na taj način zamjenjuju zrno. Gusto zbijeni micelij predstavlja tijelo plijesni. Sličnost u izgledu sklerocija i zrna omogućuje dospijevanje kontaminirane raži u hranidbeni lanac čovjeka (najčešće kruhom). Izloženost ergolinskim spojevima je široko rasprostranjena. Sve vodeće žitarice (ječam, zob, raž, sirak, pšenica, kukuruz, proso) su domaćini za C. purpurea var. Purpurea, od kojih su najznačijniji raž, ječam, zob, sirak i pšenica. Dvije najznačajnije vrste Claviceps sp. koje uzrokuju bolesti čovjeka su C. purpurea i C. fusiformis. C. fusiformis je parazit bisernog prosa u Africi i istočnoj Aziji. Ostali rodovi gljivica koji sadrže ergolinske alkaloide uključuju Aspergillus (A. clavatus, A. fumigatus), Emericella nidulans, Rhizopus nigricans i Penicillium (P. chermesinum, P. concavorugulosum, P. dierckxii). Neke više biljke također mogu sadržavati ergolinske alkaloide (slakovi). Topli i kišoviti proljetni i ljetni mjeseci pospješuju produkciju ergolinskih alkaloida. Proces pečenja kruha smanjuje njihovu količinu u sklerociju, ali ih ne uništava u potpunosti.
Raževa glavnica je u većim dozama otrovna za čovjeka i za životinju. Ako sklerociji dospiju u raž, pa se samelju u brašno, raženi kruh proizveden iz toga brašna može biti otrovan ako se konzumira dulje vremena. Proces proizvodnje hrane od žitarica smanjuje količinu ergolinskih alkaloida u hrani, po nekim podacima čak 59-100%, no i uz ovoliko smanjenje, količina ergolinskih alkaloida koji se hranom od žitarica unose u organizam varira 0,3-62 µg/kg. Od ovih koji se hranom od žitarica unose u organizam, najzastupljeniji su ergokristin, ergokristinin i ergotamin.
Kinezi su bili prvi koji su raževu glavnicu koristili u medicinske svrhe. U srednjem vijeku se koristila za zaustavljanje krvi, a od 17. stoljeća primjenjivala se u ginekologiji. Danas se derivati ergolinskih alkaloida primjenjuju u prevenciji i liječenju glavobolje (uzrokovane vaskularnim poremećajem), liječenju smanjenog tonusa maternice, senilne demencije, poremećaja ortostatske cirkulacije, neplodnosti uzrokovane povećanom koncentracijom prolaktina. Npr. tartarat ergotamina u kombinaciji s kafeinom koristi se za ublažavanje migrena i glavobolje; dihidroergotamin (intravenski pripravak) koristi se za terapiju migrenske glavobolje; bromokriptin se koristi u terapiji amenoreje, za zaustavljanje laktacije te za liječenje neuroleptičkog malignog sindroma.
Akutna toksična doza ergolinskih alkaloida mijenja se zbog individualne osjetljivosti pacijenta na vazokonstrikcijska svojstva ergotamina. Činitelji koji mijenjaju odgovor na dozu ergolinskih alkaloida su: vaskularne bolesti, preosjetljivost stijenki krvnih žila, sepsa, pušenje, pothranjenost, trudnoća, jetrene i bubrežne bolesti, bolesti štitnjače, bolesti koronarnih arterija, te istodobna primjena nekih lijekova, primjerice propranolola, oralnih kontraceptiva, derivata ksantina, eritromicina, ritonavira. Odgovor na dozu ovisi o individualnim razlikama pacijenata, o vrsti primijenjenih ergolinskih alkaloida, ali i o putu unosa lijeka (peroralno, rektalno, intramuskularno). Tako primjerice, netko može peroralno uzimati male doze ergotamina kroz dulje vrijeme a da ne dođe do pojave simptoma ergotizma (ergotizam = trovanje ergotoksinima). Intramuskularna primjena ergotamina može izazvati i pojavu akutnog infarkta miokarda. Primjena metilergonovina u novorođenčeta može dovesti do ozbiljnog poremećaja periferne cirkulacije koja zahtijeva intenzivno liječenje. Metisegid, antagonist serotonina može kod nekih osoba izazvati vazokonstrikciju i konstrikciju maternice, dok kod nekih osoba ne izaziva nikakve loše posljedice. Akutno predoziranje bromokriptinom ima relativno blage posljedice, ali višekratno predoziranje može u nekih osoba izazvati blage halucinacije.
U literaturi nema mnogo podataka o toksikokinetici pojedinih ergolinskih alkaloida i njihovih derivata. Za toksično djelovanje odgovorni su apsorpcija, distribucija, biotransformacija i uklanjanje alkaloida odnosno njihovih derivata, te interakcija s ostalim lijekovima koje bolesnik uzima. Gastrointestinalna apsorpcija većine ergolinskih alkaloida je vrlo mala, s izuzetkom bromokriptina. Terapijska koncentracija ergolinskih alkaloida obično se postiže 0,5 do 2 sata nakon ingestije. Intramuskularna primjena primjerice ergotamina, omogućuje bioraspoloživost polovice primijenjene doze (oko 47% lijeka). Poznato je da kafein povećava udio apsorbiranih ergolinskih alkaloida, a time povećava i bioraspoloživost. Distribucija ergotamina nakon intravenske primjene slijedi nakon 3 minute, s volumenom distribucije od 2 L/kg. Biotransformacija ergolodnih alkaloida (dihidrogenirani) odvija se preko oksidacije i odcjepljenja prolina u peptidnom dijelu molekule kao i cijepanja amidnih veza u molekuli. Različitost aktivnih metabolita koji zadržavaju osnovnu prstenastu strukturu produžuju trajanje djelovanja ergolinskih spojeva. Uklanjanje se gotovo u cijelosti odvija preko metabolizma u jetri odnosno preko žuči. Poluživot većine prirodnih ergolinskih alkaloida je u rasponu 1,5 – 6 sati. Otprilike 2% ergolinskih spojeva izluči se u mokraću. Opisana je interakcija nekih lijekova s ergolinskim alkaloidima. Propranolol blokira vazodilatacijski učinak epinefrina, a može uzrokovati perifernu vazokonstrikciju ergolinskih alkaloida. Makrolidni antibiotici inhibiraju metabolizam ergolinskih alkaloida, uzrokujući vazospazam i ishemiju. Oralni kontraceptivi i pušenje mogu izazvati vazospazam.
Ergotizam je posljedica bilo akutne prekomjerne ingestije, kronične primjene ergolinskih alkaloida ili ingestije malih količina ergolinskih lijekova u osoba koje su na njih preosjetljive. Rizični čimbenici za razvoj ergotizma su malnutricija (pothranjenost), febrilna stanja, sepsa, bolest koronarnih arterija, jetreno-bubrežna insuficijencija, bolest perifernih krvnih žila, pušenje, povećan krvni tlak, trudnoća, bolest štitnjače (kod pretjerane aktivnosti štitnjače odnosno prejakog izlučivanja hormona štitnjače).
Nuspojave primjene terapijskih doza ergolinskih lijekova su: mučnina, povraćanje, malaksalost, glavobolja, periferna vazokonstrikcija, spazam mišića. Metisergid uzrokuje vrtoglavicu, povraćanje, proljev, letargiju, anksioznost, nesanicu, euforiju, konfuziju. Kronična primjena metisergida uzrokuje vaskularne promjene u ekstremitetima, koronarnim arterijama i aorti, fibrozu srčanih valvula, pleure, pluća, velikih krvnih žila, osrčja.
Akcidentalna parenteralna primjena ergolinskih alkaloida u novorođenčadi (slučajna zamjena za nalokson, vitamin K) uzrokuje kožni eritem i krvarenje na ekstremitetima, preponama i genitalijama. Kožne lezije pojavljuju se drugog dana nakon primjene i traju do petoga dana. Intramuskularna ili oralna primjena ergometrina u novorođenčadi, može izazvati respiratornu depresiju, cijanozu, prekomjerno izlučivanje urina, apneju (otežano disanje). Simptomi intoksikacije pojavljuju se obično unutar jednog sata, a katkad se simptomi mogu odgoditi i do jedan sat. Smrt nastupa zbog poremećaja disanja.
Akutna toksičnost zbog ingestije ergolinskih alkaloida rijetko se događa. Opisani su neki slučajevi akutnog ergotizma koji su uzrokovali konvulzivni sindrom sa simptomima poput: halucinacije, vrtoglavice, glavobolje, mučnine/povraćanja, zvonjenje u ušima, trnaca u ekstremitetima, preosjetljivosti kože, oduzetosti polovice tijela, spazma mišića, gastrointestinalnih poremećaja. Tipično je da većina simptoma kod srčanih i gastrointestinalnih poremećaja počinju unutar 4 sata od ingestije ergotamina. Opisan je slučaj primjene povećane doze ergotamin tartarata u kombinaciji s kafeinom – Cafergot ® (Novartis) s pojavom gastritisa uz krvarenje, periferne cijanoze, moždanog edema i konačno smrti malog djeteta. Intoksikacija bromokriptinom ima blage simptome. Kod intoksikacije metisergidom simptomi se odnose na gastrointestinalni sustav i središnji živčani sustav.
Kronični ergotizam obično se pojavljuje u mladih žena koje zbog migrene konzumiraju povećane količine ergotamina. Simptomi ergotizma su simetrični, uglavnom se očituju u poremećaju periferne cirkulacije u donjim ekstremitetima. Općenito se kod kroničnog ergotizma pojavljuju sljedeći simptomi: otežano hodanje, hladne noge, bol u nogama, cijanoza, mučnina, povraćanje, abdominalna bol, edemi. U žena se dodatno pojavljuju specifični simptomi: izostanak mjesečnice, spontani pobačaj, smanjena laktacija. Nakon prestanka uzimanja ergolinskih alkaloida neki simptomi se povlače nakon 24 sata, a većina nakon nekoliko dana. Poboljšanje cirkulacije u ekstremitetima može se dokazati angiografski nakon nekoliko tjedana od prestanka primjene lijekova. Dugotrajna primjena ergotamina (npr. 6 mg/dan kroz 3 mjeseca) može uzrokovati fibrozu portalne vene i portalnu hipertenziju.
Ako je kronično trovanje uzrokovano konzumiranjem hrane kontaminirane s C. fusiformis, može se pojaviti akutna gastrointestinalna bolest: mučnina, povraćanje, somnolencija (najblaži kvantitativan poremećaj svijesti, pospanost). Simptomi se pojavljuju 1-2 sata nakon konzumiranja zagađene hrane, a nestaju nakon 48 sati. Teratogeni učinak ergotamina je vjerojatno relativno mali. Iako ima izvješća koja povezuju povećane doze ergotamina s malformacijama povezanim s vaskularnim oštećenjem, epidemiološka ispitivanja nisu potvrdila jasnu povezanost utjecaja ergotamina i oštećenja fetusa.
Liječenje ergotizma odvija se u nekoliko faza. To su stabilizacija bolesnika i dekontaminacija ergolinskih alkaloida. Na početku liječenja akutnog ergotizma najvažnije je stabilizirati bolesnika, osobito glede vitalnih funkcija (u odraslih srčani arest, srčane aritmije, smanjena količina kisika u krvi, a u novorođenčadi poremećena funkcija dišnog sustava). Antidot ne postoji. Nakon toga slijedi dekontaminacija – primjena aktivnog ugljena unutar 1-2 sata nakon ingestije >0,5 mg ergotamina/kg tjelesne mase ili >1-1,5 metisergida ili bromkriptina/kg tjelesne mase. Bolesnik nakon toga mora tijekom 24 sata pratiti moguću pojavu simptoma ergotizma. Zbog velikog volumena distribucije i male koncentracije ergotamina u krvi moguće uklanjanje ergolinskih alkaloida hemodijalizom, peritonealnom dijalizom, mokrenjem nije efektivno. Dodatnom terapijom mogu se poboljšati periferna ishemija odnosno koronarna ishemija. Izbjegavanje simultane primjene lijekova za koje se zna da mogu pospješiti toksične učinke ergolinskih alkaloida također je jedna od pomoćnih mjera.

